(Reseña publicada en la WEB de la SEPEAP el 20 de Marzo de 2007)
Se caracteriza por una disminución de la función renal en el transcurso de días o semanas con el consiguiente acumulo de productos derivados del metabolismo nitrogenado en la sangre. Los síntomas son reflejo de las alteraciones del equilibrio ácidobase e hidroelectrolítico e incluyen anorexia, nauseas y vómitos. El diagnóstico precisa la realización de los diversos test de función renal.
Etiología
Las causas de insuficiencia renal aguda pueden ser clasificadas en prerenales, renales y postrenales.
· Renal. En todos los casos se desarrollan de forma progresiva aumentos de creatinina y urea en sangre con trastornos del equilibrio hidroelectrolítico, fundamentalmente sobrecarga hídrica e hipercaliemia. La retención de fósforo con hiperfosforemia y la hipocalcemia por defecto en la hidroxilación de vitamina D son también frecuentes. Se puede originar por:
Lesión tubular aguda: tóxicos, fármacos, hipoxia.
Glomerulonefritis:
Nefropatía vascular aguda: Vasculitis, microangiopatía trombótica.
Enfermedades infiltrativas: Linfoma, leucemia, sarcoidosis.
· Postrenal. Por defecto de tipo obstructivo en el drenaje de la orina. Habitualmente se asocian con anuria.
Precipitación tubular: ácido úrico, sulfamidas, aciclovir, metotrexate, mioglobina.
Obstrucción ureteral: litiasis, micetomas, tumores, defectos congénitos.
Obstrucción vesical/uretral:
Fisiopatología
En el fallo renal agudo habitualmente se pueden identificar tres fases:
La manifestación clínica inicial puede ser aumento de peso por el edema periférico. Conforme se incrementan los niveles de metabolitos nitrogenados aparecen la anorexia, nauseas, vómitos, debilidad, mioclonias, convulsiones, asterixis, hiperreflexia, confusión y coma. La cefalea y el roce pericárdico son hallazgos habituales de pericarditis urémica. La hipervolemia puede ser causa de edema pulmonar y disnea.
Diagnóstico
Se considera que existe insuficiencia renal aguda si:
Las causas potencialmente reversibles como son las obstructivas o las prerenales deben ser excluidas en primer lugar. La valoración de los índices de función renal es de utilidad en este punto y permite hacer una correcta valoración de la evolución clínica de la insuficiencia renal.
Se caracteriza por una disminución de la función renal en el transcurso de días o semanas con el consiguiente acumulo de productos derivados del metabolismo nitrogenado en la sangre. Los síntomas son reflejo de las alteraciones del equilibrio ácidobase e hidroelectrolítico e incluyen anorexia, nauseas y vómitos. El diagnóstico precisa la realización de los diversos test de función renal.
Etiología
Las causas de insuficiencia renal aguda pueden ser clasificadas en prerenales, renales y postrenales.
· Renal. En todos los casos se desarrollan de forma progresiva aumentos de creatinina y urea en sangre con trastornos del equilibrio hidroelectrolítico, fundamentalmente sobrecarga hídrica e hipercaliemia. La retención de fósforo con hiperfosforemia y la hipocalcemia por defecto en la hidroxilación de vitamina D son también frecuentes. Se puede originar por:
Lesión tubular aguda: tóxicos, fármacos, hipoxia.
Glomerulonefritis:
- Asociada a ANCA: Wegener, poliarteritis nodosa.
- Anti-GBM: Síndrome de Goodpasture.
- Complejos immunes: LES, glomerulonefritis postinfecciosa, glomerulonefritis por crioglobulinas.
Nefropatía vascular aguda: Vasculitis, microangiopatía trombótica.
Enfermedades infiltrativas: Linfoma, leucemia, sarcoidosis.
· Postrenal. Por defecto de tipo obstructivo en el drenaje de la orina. Habitualmente se asocian con anuria.
Precipitación tubular: ácido úrico, sulfamidas, aciclovir, metotrexate, mioglobina.
Obstrucción ureteral: litiasis, micetomas, tumores, defectos congénitos.
Obstrucción vesical/uretral:
- Mecánicas: válvulas de uretra, fimosis.
- Neurogénica: anticolinérgicos, lesión de motoneurona inferior y superior.
Fisiopatología
En el fallo renal agudo habitualmente se pueden identificar tres fases:
- Fase prodrómica: Existe producción normal de orina. Su duración es variable dependiendo de las causas.
- Fase oligúrica: Con duración media de 10-14 días. La duración de esta fase se asocia con los requerimientos de diálisis.
- Fase postoligúrica. En esta fase la producción de orina retorna progresivamente a su ritmo normal. La disfunción tubular puede persistir mas tiempo y manifestarse con un aclaramiento masivo de sodio y poliuria por falta de respuesta a la vasopresina.
La manifestación clínica inicial puede ser aumento de peso por el edema periférico. Conforme se incrementan los niveles de metabolitos nitrogenados aparecen la anorexia, nauseas, vómitos, debilidad, mioclonias, convulsiones, asterixis, hiperreflexia, confusión y coma. La cefalea y el roce pericárdico son hallazgos habituales de pericarditis urémica. La hipervolemia puede ser causa de edema pulmonar y disnea.
Diagnóstico
Se considera que existe insuficiencia renal aguda si:
- Aumento de urea superior a 10 mg/dl/día.
- Creatinina sérica es superior a 1 mg/dl o asciende más de 0.20.5 mg/dl/día. Ascensos mayores de 2 mg/dl/día sugieren rabdomiolisis.
- Existe oliguria, entendiéndose como la producción de orina de menos de 25 ml/Kg/día, si bien puede existir fallo renal en presencia de una producción normal de orina.
Las causas potencialmente reversibles como son las obstructivas o las prerenales deben ser excluidas en primer lugar. La valoración de los índices de función renal es de utilidad en este punto y permite hacer una correcta valoración de la evolución clínica de la insuficiencia renal.
Prerrenal
|
Renal
|
Postrenal
|
|
Osmolaridad urinaria/plasmática
|
>1.5
|
1-1.5
|
1-1.5
|
Sedimento urinario
|
Normal
|
Hematuria
|
Normal/Hematuria
|
Na orina (mEq/l)
|
<20
|
20-40
|
>40
|
Na orina/Na plasma
|
0.25 ± 0.15
|
0.5 ± 0.2
|
|
Urea orina/Urea plasma
|
29 ± 18
|
5.8 ± 3
|
|
Cr orina/ Cr plasma
|
29 ± 16
|
10 ± 4
|
|
FENa/Cr
|
<
0.01
|
0.01-0.02
|
>0.04
|
Índice de fallo renal
|
<
1
|
<1- > 2
|
>2
|
Cociente osmolar
|
>
1
|
<1
|
Valoración
de la función glomerular (velocidad de filtrado glomerular).
En el recién nacido
alcanza valores del 20‑40% de los del adulto. Su medida requiere pruebas de
aclaramiento, en las que se determina el volumen aclarado de una sustancia
por el riñón en un minuto. Las más empleadas son:
- Aclaramiento de creatinina.
- Aclaramiento de urea.
- Aclaramiento de inulina.
De ellas la más
utilizada es el aclaramiento de creatinina (AC), si bien durante el período
neonatal hemos de observar la interferencia de la creatinina (Cr) materna
hasta el 5º día de vida.
En neonatos la superficie corporal aproximada sería de 0.14 m2 para niños de 2 Kg; 0.16 m2 en niños de 2.5 Kg y de 019 m2 en mayores de 3 Kg.
Los valores normales de aclaramiento de creatinina serían:
- Recién nacido (2830 semanas): 10.2 a 20 ml/min/1.73 m2.
- Recién nacido (3137 semanas): 2530 ml/min/1.73 m2.
- Recién nacido (>37 semanas): 3540 ml/min/1.73 m2..
- Lactante hasta los 2 meses: 6575 ml/min/1.73 m2.
- Adultos: 97137 ml/min/1.73 m2 en hombres y 88128 ml/min/1.73 m2 en mujeres
Cuando no se dispone de volumen urinario de 24 horas se puede controlar la velocidad de filtrado glomerular a partir de las siguientes fórmulas:
Menores de 1 año:
Entre 1 y 13 años:
Mayores de 13 años:
Expresando la talla en cm y la Cr plasmática en mg/dl; el resultado se expresa en ml/min/1.73 m2.
Valoración de la función tubular.
Excreción fraccionada de sodio/Urea (FENa / Urea). Se expresa como porcentaje del sodio filtrado; si lo referimos a la relación con la urea o con el aclaramiento de creatinina aumenta su exactitud.
Excreción fraccionada de sodio/creatinina. Los valores normales en el recien nacido (3740 semanas) son de 0.19 (DS 0.032).
Excreción fraccionada de potasio/creatinina (FEK/Cr). Los valores normales corresponden a un 20 % de lo filtrado.
Excreción fraccionada de bicarbonato/Creatinina. Los valores normales varían en razón a los valores de bicarbonato plasmático. Si el bicarbonato en plasma es de 18 mEq/L su valor es de 0.4 %. Si el bicarbonato en plasma es de 24 mEq/L su valor es del 5 %.
Reabsorción tubular de fosfato. Valores normales del 7585 %.
Valoración de la función glomerulartubular. Se valora mediante el índice de fallo renal (IFR). Un IFR mayor de 1 indica insuficiencia renal de origen renal.
Cociente osmolar. Relaciona la osmolaridad urinaria y plasmática, ambas expresadas en mOsm/L. Si la relación es menor de 1 = I.R. intrínseca. Si la relación es mayor de 1 = I.R.A. prerrenal.
Aclaramiento de agua libre. Cantidad de agua que debe ser sustraída o añadida a la orina para convertirla en isoosmótica con el plasma. En condiciones normales el aclaramiento de agua libre es negativo, ya que se excretan más solutos que agua. Su cálculo precisa el conocimiento previo de aclaramiento osmolar (AO). Donde V es el volumen urinario en ml/min.
El aclaramiento de agua libre viene dado por la expresión: AAL = V _ A.O.
Si su valor es negativo, ello nos indica restricción hídrica. Si es positivo indica diuresis acuosa.
Prueba de sobrecarga.
Podemos recurrir a ella siempre que no existan signos de sobrecarga circulatoria y la presión venosa central no esté alterada. Efectuamos una sobrecarga líquida con S. glucosado al 10 % y 30 mEq/L de ClNa, pasando 20 ml/Kg en 1 o 2 horas. Si no se restablece una diuresis adecuada añadimos furosemida (23 mg/Kg) IV. Si persiste la oliguria y/o urea es mayor de 40 mg/dl durante las 24 horas siguientes, se debe determinar el cociente osmolar y la excreción fraccionada de sodio. Si el cociente osmolar es inferior a 1 y la FENa es mayor de 3 se trata de una I.R. intrínseca.
Sedimento y sistemático de orina.
La realización de un sedimento de orina puede aproximarnos al diagnóstico etiológico de la insuficiencia renal. Los cilindros granulosos y celulares se observan en la insuficiencia renal prerenal y ocasionalmente en las formas obstructivas. En las lesiones tubulares renales el sedimento habitualmente contiene células tubulares y cilindros de células tubulares. La presencia de eosinófiulos en el sedimento sugiere nefritis tubulointersticial alérgica. Los cilíndros hemáticos sugieren glomerulonefritis o vasculitis. La existencia de proteinuria sugiere causa renal.
Ecografía.
La ecografía permite determinar el grado de inflamación renal y la existencia de dilatación en pelvis renal y uréter. Un volumen postmiccional de orina identificado por ecografía superior a 200 ml puede sugerir una causa obstructiva, aunque la sensibilidad de la ecografía para diagnosticar obstrucciones en uretra es baja.
Tratamiento
Corrección de la volemia.
Líquidos a aportar = (Pérdidas insensibles _ 20 ml/Kg/día) + (Pérdidas sensibles _ 10 ml/Kg por cada 0 C superior a los 370 C) + Diuresis.
Expansores plasmáticos mas dopamina a dosis dopaminérgicas o betaadrenérgicas. Puede requerirse la asociación de furosemida a 2 mg/Kg/dosis hasta un máximo de 10 mg/Kg/ dia.
Tratamiento dietético.
· Calorías. En el recién nacido un mínimo de 40 Kcal/m2/día. En el niño 400 Kcal/m2/día.
· Proteínas. Máximo de 0.5_1 g/Kg/día. Si se administran aminoácidos darlos a la dosis de 50 mg/Kg/día.
Corrección de los trastornos metabólicos.
Hiperpotasemia:
- Entre 5.5 _ 6.5 mEq/L.: Resin-calcio 1_2 g/Kg/dosis en S. glucosado al 10% (3 ml por gramo de resina en forma de enema de retención o sonda nasogástrica).
- Entre 6.5_7.5 mEq/L: Gluconato cálcico al 10% (0.5_1 ml/Kg/ dosis) en 2 minutos y/o Bicarbonato sódico 1/2 M. (2_3 mEq/Kg/ dosis) en 10 minutos y/o Glucosa al 50 % (1 ml/Kg) + Insulina (1 U/5 g de glucosa) en 15 minutos. Si estas medidas no dan resultado en 2_3 horas proceder a diálisis peritoneal.
Hiponatremia:
· < 130 mEq/L y asintomática se hará restricción de líquidos.
· < 115 mEq/L y sintomática. Se hará restricción hídrica, administrando el 25% de las necesidades basales como máximo. Administrar Na+ a razón de 8 mEq/Kg/hora, valorando horariamente la respuesta bioquímica e hídrica. Si existe una depleción sódica (Na<120 mEq/l), se corregirá el Na hasta 125 mEq/l de acuerdo a la expresión: Na (mEq) = (125 _ Na real) x 0.6 x Kg.
Hipocalcemia: Se administra gluconato cálcico al 10 % (0.5 ml/Kg/dosis.
Acidosis metabólica: Si el bicarbonato plasmático es superior a 15 mEq/L no se trata, por su efecto protector de convulsiones. Si el pH < 7.10 y/o el bicarbonato es menor de 15 mEq/L se administra bicarbonato sódico hasta conseguir un pH de 7.2, calculado según la expresión: 0.3 x Kg x (12-CO3HNa)
Hiperfosforemia: Se administra hidróxido de aluminio: 1 ml/Kg/día (VO).
Hipomagnesemia: Se utiliza sulfato de magnesio: 0.1 ml/Kg/día (IM).
Tratamiento de la hipertensión arterial.
Restricción hidrosalina.
Furosemida: 2 mg/Kg/ dosis, a ritmo de 4 mg/min., se puede repetir con 10 mg/Kg, si no se obtiene aumento de la diuresis no administrar mas furosemida por su efecto ototóxico y administrar manitol 0.5 g/Kg en 30 minutos.
En las crisis hipertensivas se administra en primer lugar hidralazina 0.2 mg/Kg IV/IM (máximo 4 dosis al día). Diazóxido: 5 mg/Kg (IV rápido). Nifedipina: 0.25_0.5 mg/ Kg/dosis (sublingual). Labetalol: 1_4 mg/Kg/ hora en infusión IV.
Indicaciones de diálisis peritoneal.
Insuficiencia renal aguda con oligoanuria (diuresis < 0.5 ml/Kg/h) que no responde a diuréticos y que puede acompañarse de:
- Hipervolemia.
- Hipertensión arterial.
- Insuficiencia cardiaca.
- Derrame pleural o pericárdico.
- Anasarca.
Alteraciones electrolíticas y del pH sanguíneo:
Hiperkaliemia venosa mayor de 7 mEq/L y/o alteraciones en ECG.
Acidosis metabólica severa.
Hipernatremia mayor de 170 mEq/L.
Urea plasmática en general mayor de 240 mg/dl y se prevee una evolución prolongada de la I.R.
Síndrome hemolítico urémico.
Intoxicación por tóxicos dializables en peritoneo (los tóxicos liposolubles o que se unen fuertemente a proteínas plasmáticas no son dializables por este método).
Técnica de diálisis peritoneal.
Vaciamiento vesical por sondaje.
Sedación.
Anestesia local de la pared abdominal.
Incisión pequeña de ± 0.5 cm, disecando tejido celular y fascia.
Introducir aguja y pasar 30 ml/Kg de líquido de diálisis caliente para provocar ascitis.
Introducir catéter con el estilete hasta atravesar peritoneo. Quitar el estilete y dirigir el cateter oblicuamente hacia fosa iliaca izquierda.
Realizar intercambio de prueba y fijar.
Control y seguimiento de una diálisis peritoneal.
El líquido de diálisis estándar o isotónico presenta una composición aproximada de: dextrosa 1.5 g/dl, sodio a 134140 mEq/l, cloro de 101 a 103 mEq/l,lactato de 36 a 40 g/l, calcio 4 mEq/l, magnesio 1.5 mEq/l, no contiene potasio y su osmolalidad es de 360375 mOsm/Kg.
El volumen de cada intercambio es de 3050 ml/Kg, según la tolerancia del paciente, cada intercambio debe durar alrededor de 1 hora entre entrada, permanencia y salida. En lactantes pequeños pueden requerirse sesiones de 6 pases en unas 8 horas cada 2448 horas.
En general el gradiente osmótico deseable debe ser 3050 mOsm/Kg de gradiente en favor del líquido de diálisis. En situaciones en que interese hacer balances más negativos puede requerirse incrementar la osmolalidad del líquido de diálisis. Las soluciones comerciales que no contienen potasio, deben ser suplementadas a partir del 45º pase con potasio a 4 mEq/l.
Debe añadirse heparina a 20 mg/l, cefalotina 1 g/Kg, Novocaina 3 ml/l y cualquier otra sustancia específica indicada (albúmina al 5 % en la intoxicación barbitúrica o salicílica).
En las situaciones de hipernatremia grave el gradiente sódico debe ser de 20 mEq/l mayor en el plasma que en el líquido de diálisis.
Se aconsejan controles analíticos cada 12 horas.
Cualquier balance negativo que no sea deseable se corregirá con aumento de los aportes parenterales. Si el balance intradiálisis de varios intercambio positivo, añadir glucosa a razón de 1 g=5.5 mOsm. hasta hacerlos negativos.
Complicaciones de la diálisis peritoneal.
Hipoproteinemia.
Peritonitis. Aumentar ritmo de los pases y osmolaridad, añadir antisépticos (BetadineR, 10 ml/L de solución).
Perforación de víscera hueca.
Implantación preperitoneal, con fugas, drenaje insuficiente. Esta indicado cambiar el catéter.
Hipervolemia por retención de líquidos.
Hipovolemia e hipernatremia.
Hipocalcemia.
Alcalosis metabólica.
Síndrome de desequilibrio. Prevenir con descensos osmóticos suaves.
Dr. José Uberos Fernández


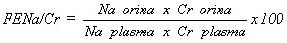





Comentarios
Publicar un comentario